آنچه در این مطلب خواهید خواند
- هورمونها و گیرندههای هورمونی چیستند؟
- هورموندرمانی چیست؟
- چه نوع هورموندرمانی برای سرطان پستان استفاده میشود؟
- هورموندرمانی چگونه برای درمان سرطان پستان استفاده میشود؟
- آیا میتوان از هورموندرمانی برای پیشگیری از سرطان پستان استفاده کرد؟
- عوارض جانبی هورموندرمانی چیست؟
- آیا داروهای دیگر میتوانند با هورموندرمانی تداخل داشته باشند؟
- منابع منتخب
هورمونها و گیرندههای هورمونی چیستند؟
هورمونها موادی هستند که به عنوان پیامرسانهای شیمیایی در بدن عمل میکنند. آنها بر عملکرد سلولها و بافتها در نقاط مختلف بدن تأثیر میگذارند و اغلب از طریق جریان خون به اهداف خود میرسند.
هورمونهای استروژن و پروژسترون توسط تخمدانها در زنان قبل از یائسگی و توسط برخی بافتهای دیگر، از جمله چربی و پوست، در زنان قبل و بعد از یائسگی و همچنین در مردان تولید میشوند. استروژن باعث ایجاد و حفظ ویژگیهای جنسی زنانه و رشد استخوانهای بلند میشود. پروژسترون در چرخه قاعدگی و بارداری نقش دارد.
استروژن و پروژسترون همچنین رشد برخی از سرطانهای پستان را که سرطانهای پستان حساس به هورمون (یا وابسته به هورمون) نامیده میشوند، تقویت میکنند. سلولهای سرطان پستان حساس به هورمون حاوی پروتئینهایی به نام گیرندههای هورمونی ( گیرندههای استروژن یا ER و گیرندههای پروژسترون یا PR) هستند که وقتی هورمونها به آنها متصل میشوند، فعال میشوند. گیرندههای فعال شده باعث ایجاد تغییراتی در بیان ژنهای خاص میشوند که میتوانند رشد سلول را تحریک کنند.
برای تعیین اینکه آیا سلولهای سرطان پستان حاوی گیرندههای هورمونی هستند یا خیر، پزشکان نمونههایی از بافت تومور را که با جراحی برداشته شدهاند، آزمایش میکنند. اگر سلولهای تومور حاوی گیرندههای استروژن باشند، سرطان گیرنده استروژن مثبت (ER مثبت)، حساس به استروژن یا پاسخگو به استروژن نامیده میشود. به طور مشابه، اگر سلولهای تومور حاوی گیرندههای پروژسترون باشند، سرطان گیرنده پروژسترون مثبت (PR یا PgR مثبت) نامیده میشود. تومورهای پستانی که حاوی گیرندههای استروژن و/یا پروژسترون هستند، گاهی اوقات گیرنده هورمون مثبت (HR مثبت) نامیده میشوند. اکثر سرطانهای پستان ER مثبت، PR مثبت نیز هستند.
سرطانهای پستانی که فاقد گیرندههای استروژن (ER) هستند ، ER منفی نامیده میشوند و اگر فاقد هر دو گیرنده استروژن و پروژسترون باشند، ممکن است HR منفی نامیده شوند.
تقریباً 67 تا 80 درصد سرطانهای پستان در زنان ER مثبت هستند (1، 2). تقریباً 90 درصد سرطانهای پستان در مردان ER مثبت و تقریباً 80 درصد PR مثبت هستند (3).
هورموندرمانی چیست؟
هورموندرمانی (که به آن غدد درون ریز درمانی نیز گفته میشود) با مسدود کردن توانایی بدن در تولید هورمون یا با تداخل در اثرات هورمونها بر سلولهای سرطان پستان، رشد تومورهای حساس به هورمون را کند یا متوقف میکند. تومورهایی که به هورمون حساس نیستند، گیرندههای هورمونی ندارند و به هورموندرمانی پاسخ نمیدهند.
هورموندرمانی برای سرطان پستان نباید با هورموندرمانی یائسگی (MHT) اشتباه گرفته شود- درمان با استروژن به تنهایی یا همراه با پروژسترون برای کمک به تسکین علائم یائسگی- این دو نوع درمان اثرات متضادی دارند: هورموندرمانی برای سرطان پستان، رشد سرطان پستان HR مثبت را مسدود میکند، در حالی که MHT میتواند رشد سرطان پستان HR مثبت را تحریک کند. به همین دلیل، وقتی زنی که MHT مصرف میکند، به سرطان پستان HR مثبت مبتلا میشود، معمولاً از او خواسته میشود که درمان را متوقف کند.
چه نوع هورموندرمانی برای سرطان پستان استفاده میشود؟
چندین استراتژی برای درمان سرطان پستان حساس به هورمون استفاده میشود:
مسدود کردن عملکرد تخمدان: از آنجا که تخمدانها منبع اصلی استروژن در زنان قبل از یائسگی هستند، سطح استروژن در این زنان میتواند با از بین بردن یا سرکوب عملکرد تخمدان کاهش یابد. مسدود کردن عملکرد تخمدان، تخریب تخمدان نامیده میشود.
برداشتن تخمدان میتواند به صورت جراحی در یک عمل جراحی برای برداشتن تخمدانها (به نام اوفورکتومی) یا با پرتودرمانی انجام شود. این نوع برداشتن تخمدان معمولاً دائمی است.
از طرف دیگر، عملکرد تخمدان را میتوان به طور موقت با درمان با داروهایی به نام آگونیست هورمون آزادکننده گنادوتروپین (GnRH) که به عنوان آگونیست هورمون آزادکننده هورمون لوتئینیزه کننده (LHRH) نیز شناخته میشوند، سرکوب کرد. این داروها با تقلید از GnRH، در سیگنالهایی که تخمدانها را برای تولید استروژن تحریک میکنند، اختلال ایجاد میکنند.
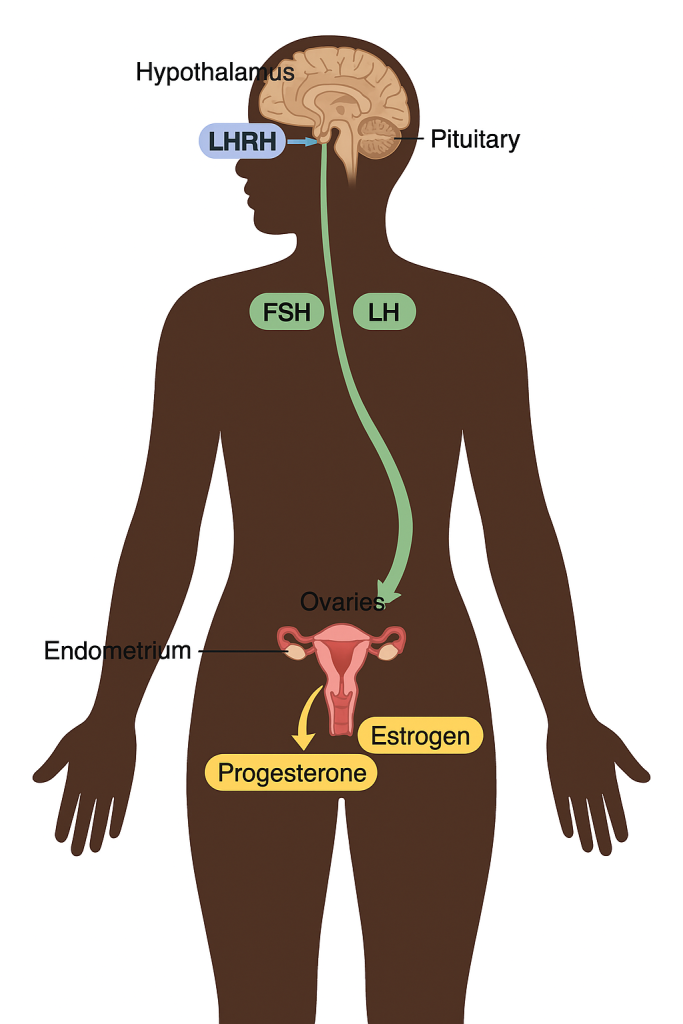
نمونههایی از داروهای سرکوب تخمدان عبارتند از گوسرلین (زولادکس) و لوپرولید (لوپرون).
مسدود کردن تولید استروژن: داروهایی به نام مهارکنندههای آروماتاز برای مسدود کردن فعالیت آنزیمی به نام آروماتاز استفاده میشوند که بدن از آن برای تولید استروژن در تخمدانها و سایر بافتها استفاده میکند. مهارکنندههای آروماتاز در درجه اول در زنان یائسه استفاده میشوند زیرا تخمدانها در زنان قبل از یائسگی، آروماتاز زیادی تولید میکنند که مهارکنندهها نمیتوانند به طور مؤثر آن را مسدود کنند. با این حال، اگر این داروها همراه با دارویی که عملکرد تخمدان را سرکوب میکند، تجویز شوند، میتوانند در زنان قبل از یائسگی نیز استفاده شوند.
نمونههایی از مهارکنندههای آروماتاز که توسط سازمان غذا و داروی آمریکا (FDA) تأیید شدهاند عبارتند از آناستروزول (آریمیدکس) و لتروزول (فمارا)، که هر دو به طور موقت آروماتاز را غیرفعال میکنند، و اگزمستان (آروماسین)، که به طور دائم آروماتاز را غیرفعال میکند.
مسدود کردن اثرات استروژن: چندین نوع دارو در توانایی استروژن در تحریک رشد سلولهای سرطان پستان اختلال ایجاد میکنند:
- تعدیلکنندههای انتخابی گیرنده استروژن (SERM) به گیرندههای استروژن متصل میشوند و از اتصال استروژن جلوگیری میکنند. نمونههایی از SERM های تأیید شده توسط FDA برای درمان سرطان پستان، تاموکسیفن (Nolvadex) و تورمیفن (Fareston) هستند.
از آنجا که آنها به گیرندههای استروژن متصل میشوند، SERM ها به طور بالقوه نه تنها میتوانند فعالیت استروژن را مسدود کنند (با جلوگیری از اتصال استروژن به گیرنده آن)، بلکه بسته به محل بیان آنها در بدن، اثرات استروژن را نیز تقلید میکنند. به عنوان مثال، تاموکسیفن اثرات استروژن را در بافت پستان مسدود میکند، اما مانند استروژن در رحم و استخوان عمل میکند. - سایر داروهای ضد استروژن، مانند فولوسترانت (Faslodex)، به روشی تا حدودی متفاوت برای مسدود کردن اثرات استروژن عمل میکنند. فولوسترانت مانند SERMها به گیرنده استروژن متصل میشود و به عنوان یک مسدودکننده استروژن عمل میکند. با این حال، برخلاف SERMها، فولوسترانت از استروژن تقلید نمیکند. به همین دلیل، به آن یک ضد استروژن خالص میگویند. علاوه بر این، هنگامی که فولوسترانت به گیرنده استروژن متصل میشود، گیرنده برای تخریب هدف قرار میگیرد.
هورموندرمانی چگونه برای درمان سرطان پستان استفاده میشود؟
سه روش اصلی برای هورموندرمانی جهت درمان سرطان پستان حساس به هورمون وجود دارد:
درمان کمکی برای سرطان پستان در مراحل اولیه: تاموکسیفن برای درمان هورمونی کمکی زنان (و مردان) قبل و بعد از یائسگی مبتلا به سرطان پستان در مراحل اولیه ER مثبت توسط سازمان غذا و داروی آمریکا (FDA) تأیید شده است و مهارکنندههای آروماتاز آناستروزول، لتروزول و اگزمستان برای این استفاده در زنان یائسه تأیید شدهاند.
تحقیقات نشان داده است زنانی که حداقل 5 سال پس از جراحی سرطان پستان ER مثبت در مراحل اولیه، تحت درمان کمکی با تاموکسیفن قرار میگیرند، خطر عود سرطان پستان، از جمله سرطان پرستان جدید در پستان دیگر، و خطر مرگ در 15 سال کاهش مییابد (4).
تا همین اواخر، اکثر زنانی که برای کاهش احتمال عود سرطان پستان، هورموندرمانی کمکی دریافت میکردند، به مدت 5 سال هر روز تاموکسیفن مصرف میکردند. با این حال، با معرفی هورموندرمانیهای جدیدتر (یعنی مهارکنندههای آروماتاز)، که برخی از آنها در کارآزماییهای بالینی با تاموکسیفن مقایسه شدهاند، رویکردهای اضافی به هورموندرمانی رایج شده است (5-7).
برای مثال، برخی از زنان ممکن است به جای تاموکسیفن، هر روز به مدت 5 سال یک مهارکننده آروماتاز مصرف کنند. برخی دیگر از زنان ممکن است پس از 5 سال مصرف تاموکسیفن، درمان اضافی با مهارکننده آروماتاز دریافت کنند. در نهایت، برخی از زنان ممکن است پس از 2 یا 3 سال مصرف تاموکسیفن، به یک مهارکننده آروماتاز روی آورند و در مجموع 5 سال یا بیشتر هورموندرمانی انجام دهند. تحقیقات نشان داده است که برای زنان یائسهای که برای سرطان پستان در مراحل اولیه درمان شدهاند، درمان کمکی با مهارکننده آروماتاز در مقایسه با تاموکسیفن کمکی، خطر عود را کاهش داده و بقای کلی را بهبود میبخشد (8).
برخی از زنان قبل از یائسگی مبتلا به سرطان پستان ER مثبت در مراحل اولیه ممکن است سرکوب تخمدان به همراه یک مهارکننده آروماتاز داشته باشند که مشخص شده است که میزان رهایی از عود در این روش نسبت به سرکوب تخمدان به همراه تاموکسیفن یا تاموکسیفن به تنهایی بالاتر است (9).
مردانی که در مراحل اولیه سرطان پستان ER مثبت هستند و تحت درمان کمکی قرار میگیرند، معمولاً ابتدا با تاموکسیفن درمان میشوند. افرادی که با مهارکننده آروماتاز درمان میشوند، معمولاً آگونیست GnRH نیز مصرف میکنند.
تصمیمگیری در مورد نوع و مدت زمان هورموندرمانی کمکی پیچیده است و باید به صورت فردی و با مشورت یک متخصص انکولوژی انجام شود.
درمان سرطان پستان پیشرفته یا متاستاتیک: چندین نوع هورموندرمانی برای درمان سرطان پستان متاستاتیک یا عودکننده حساس به هورمون تأیید شده است. هورموندرمانی همچنین یک گزینه درمانی برای سرطان پستان ER مثبت است که پس از درمان در پستان، دیواره قفسه سینه یا غدد لنفاوی مجاور عود کرده است (که به آن عود موضعی نیز گفته میشود).
دو SERM، تاموکسیفن و تورمیفن، برای درمان سرطان پستان متاستاتیک تأیید شدهاند. فولوسترانت آنتیاستروژن برای زنان یائسه مبتلا به سرطان پستان متاستاتیک ER مثبت که پس از درمان با سایر آنتیاستروژنها گسترش یافته است، تأیید شده است (10). فولوسترانت همچنین برای زنان یائسه مبتلا به سرطان پستان پیشرفته موضعی یا متاستاتیک HR مثبت، HER2 منفی که قبلاً با هورموندرمانی درمان نشدهاند، تأیید شده است (11). علاوه بر این، ممکن است در زنان قبل از یائسگی که تحت عمل جراحی برداشتن تخمدان قرار گرفتهاند، استفاده شود .
مهارکنندههای آروماتاز، آناستروزول و لتروزول، برای زنان یائسه به عنوان درمان اولیه برای سرطان پستان حساس به هورمون متاستاتیک یا پیشرفته موضعی تأیید شدهاند (12، 13). هر دوی این داروها و مهارکننده آروماتاز، اگزمستان، نیز برای درمان زنان یائسه مبتلا به سرطان پستان پیشرفته که بیماری آنها پس از درمان با تاموکسیفن بدتر شده است، تأیید شدهاند (14). مردان مبتلا به سرطان پستان پیشرفته که با یک مهارکننده آروماتاز درمان میشوند، آگونیست GnRH نیز دریافت میکنند.
برخی از زنان مبتلا به سرطان پستان پیشرفته با ترکیبی از هورموندرمانی و یکی از چندین درمان هدفمند زیر درمان میشوند:
- پالبوسیکلیب (Ibrance) برای استفاده در ترکیب با لتروزول به عنوان درمان اولیه برای درمان سرطان پستان پیشرفته یا متاستاتیک HR مثبت، HER2 منفی در زنان یائسه تأیید شده است. پالبوسیکلیب دو کیناز وابسته به سیکلین (CDK4 و CDK6) را مهار میکند که به نظر میرسد رشد سلولهای سرطان پستان HR مثبت را افزایش میدهند (15).
پالبوسیکلیب همچنین برای استفاده در ترکیب با فولوسترانت برای درمان زنان یائسه مبتلا به سرطان پستان پیشرفته یا متاستاتیک HR مثبت، HER2 منفی که سرطان آنها پس از درمان با هورموندرمانی دیگری بدتر شده است، تأیید شده است (16). - Abemaciclib (Verzenio)، یکی دیگر از مهارکنندههای CDK4 و CDK6، برای استفاده در ترکیب با fulvestrant برای زنان یائسه مبتلا به سرطان پستان پیشرفته یا متاستاتیک HR مثبت، HER2 منفی که بیماری آنها پس از درمان با هورموندرمانی پیشرفت کرده است (17)، تأیید شده است. Abemaciclib همچنین برای استفاده به تنهایی برای زنان و مردان مبتلا به سرطان پستان پیشرفته یا متاستاتیک HR مثبت، HER2 منفی که بیماری آنها پس از درمان با هورموندرمانی و شیمیدرمانی قبلی برای بیماری متاستاتیک بدتر شده است (18)، تأیید شده است.
Abemaciclib همچنین برای استفاده با یک مهارکننده آروماتاز به عنوان هورموندرمانی خط اول در زنان یائسه مبتلا به سرطان پستان پیشرفته یا متاستاتیک HR مثبت، HER2 منفی تأیید شده است. - ریبوسیکلیب (Kisqali)، یکی دیگر از مهارکنندههای CDK4/6، برای استفاده در ترکیب با یک مهارکننده آروماتاز در زنان یائسه مبتلا به سرطان پستان پیشرفته یا متاستاتیک HR مثبت، HER2 منفی که با هورموندرمانی درمان نشدهاند، تأیید شده است (19، 20).
ریبوسیکلیب همچنین برای استفاده در ترکیب با فولوسترانت در زنان یائسه مبتلا به سرطان پستان پیشرفته یا متاستاتیک HR مثبت، HER2 منفی که با هورموندرمانی درمان نشدهاند یا بیماری آنها در طول درمان با هورموندرمانی بدتر شده است، تأیید شده است (21). - لاپاتینیب (Tykerb) برای استفاده در ترکیب با لتروزول برای درمان سرطان پستان متاستاتیک HR مثبت و HER2 مثبت در زنان یائسه که هورموندرمانی برای آنها تجویز شده است، تأیید شده است. این دارو یک مهارکننده کوچک مولکول تیروزین کینازهای HER2 و EGFR است.
- آلپلیسیب (پیکری) برای درمان سرطان پستانی که HR مثبت و HER2 منفی است و جهشی در ژن PIK3CA دارد، تأیید شده است . این دارو به همراه فولوسترانت برای درمان زنان یائسه و مردانی که سرطان پستان آنها پیشرفته یا متاستاتیک است و در طول یا بعد از درمان با هورموندرمانی بدتر شده است، استفاده میشود (22).
- برخی از زنان مبتلا به سرطان پستان پیشرفته که HER2 و HR مثبت دارند، ممکن است هورموندرمانی به همراه تراستوزوماب با یا بدون پرتوزوماب دریافت کنند (23).
درمان نئوادجوانت سرطان پستان: استفاده از هورموندرمانی برای درمان سرطان پستان به منظور کاهش اندازه تومور قبل از جراحی (درمان نئوادجوانت) در آزمایشات بالینی مورد مطالعه قرار گرفته است (24). این آزمایشات نشان داده است که هورموندرمانی نئوادجوانت – به ویژه با مهارکنندههای آروماتاز – میتواند در کاهش اندازه تومورهای پستان در زنان یائسه مؤثر باشد، اما هنوز مشخص نیست که در زنان قبل از یائسگی چقدر مؤثر است.
هورموندرمانی گاهی اوقات برای درمان نئوادجوانت سرطان پستان HR مثبت در زنان یائسه که نمیتوانند شیمیدرمانی را تحمل کنند یا زمانی که جراحی باید به تأخیر بیفتد، استفاده میشود.
آیا میتوان از هورموندرمانی برای پیشگیری از سرطان پستان استفاده کرد؟
بله. اکثر سرطانهای پستان ER مثبت هستند و آزمایشهای بالینی بررسی کردهاند که آیا میتوان از هورموندرمانی برای پیشگیری از سرطان پستان در زنانی که در معرض خطر ابتلا به این بیماری هستند، استفاده کرد یا خیر.
یک کارآزمایی بالینی تصادفی بزرگ تحت حمایت NCI به نام کارآزمایی پیشگیری از سرطان پستان نشان داد که مصرف تاموکسیفن به مدت 5 سال، خطر ابتلا به سرطان تهاجمی پستان را در زنان یائسهای که در معرض خطر بیشتری بودند، حدود 50٪ کاهش میدهد (25). پیگیری طولانیمدت یک کارآزمایی تصادفی دیگر، مطالعه بینالمللی مداخله سرطان پستان، نشان داد که 5 سال درمان با تاموکسیفن، بروز سرطان پستان را حداقل به مدت 20 سال کاهش میدهد (26). یک کارآزمایی تصادفی بزرگ بعدی، مطالعه تاموکسیفن و رالوکسیفن، که آن هم توسط NCI حمایت مالی شد، نشان داد که 5 سال مصرف رالوکسیفن (یک SERM) خطر سرطان پستان را در چنین زنانی حدود 38٪ کاهش میدهد (27).
در نتیجه این آزمایشات، هم تاموکسیفن و هم رالوکسیفن توسط سازمان غذا و داروی آمریکا (FDA) برای کاهش خطر ابتلا به سرطان پستان در زنانی که در معرض خطر بالای ابتلا به این بیماری هستند، تأیید شدهاند. تاموکسیفن صرف نظر از وضعیت یائسگی برای این منظور تأیید شده است. رالوکسیفن فقط برای استفاده در زنان یائسه تأیید شده است.
همچنین مشخص شده است که دو مهارکننده آروماتاز -اگزمستان و آناستروزول- خطر ابتلا به سرطان پستان را در زنان یائسهای که در معرض خطر بالای ابتلا به این بیماری هستند، کاهش میدهند. پس از 3 سال پیگیری در یک کارآزمایی تصادفی، زنانی که اگزمستان مصرف میکردند، 65٪ کمتر از کسانی که دارونما مصرف میکردند، به سرطان پستان مبتلا شدند (28). پس از 7 سال پیگیری در یک کارآزمایی تصادفی دیگر، زنانی که آناستروزول مصرف میکردند، 50٪ کمتر از کسانی که دارونما مصرف میکردند، به سرطان پستان مبتلا شدند (29). هم اگزمستان و هم آناستروزول توسط FDA برای درمان زنان مبتلا به سرطان پستان ER مثبت تأیید شدهاند. اگرچه هر دو برای پیشگیری از سرطان پستان نیز استفاده میشوند، اما هیچکدام به طور خاص برای این منظور تأیید نشدهاند.
عوارض جانبی هورموندرمانی چیست؟
عوارض جانبی هورموندرمانی تا حد زیادی به داروی خاص یا نوع درمان بستگی دارد (7). فواید و مضرات مصرف هورموندرمانی باید برای هر فرد به دقت سنجیده شود. یک استراتژی رایج برای تغییر درمان کمکی که در آن بیماران به مدت 2 یا 3 سال تاموکسیفن مصرف میکنند و به دنبال آن به مدت 2 یا 3 سال یک مهارکننده آروماتاز مصرف میکنند، ممکن است بهترین تعادل بین فواید و مضرات این دو نوع هورموندرمانی را ایجاد کند (30).
گرگرفتگی، تعریق شبانه و خشکی واژن از عوارض جانبی شایع همه هورموندرمانیها هستند. هورموندرمانی همچنین ممکن است چرخه قاعدگی را در زنان قبل از یائسگی مختل کند.
عوارض جانبی کمتر شایع اما جدی داروهای هورموندرمانی در زیر فهرست شده است.
تاموکسیفن
- خطر لخته شدن خون ، به ویژه در ریهها و پاها
- سکته
- آب مروارید
- سرطان آندومتر و سارکوم رحم
- از دست دادن استخوان در زنان قبل از یائسگی، اما بدون افزایش خطر شکستگی
- نوسانات خلقی، افسردگی و از دست دادن میل جنسی
- در مردان: سردرد، حالت تهوع، استفراغ، بثورات پوستی، ناتوانی جنسی و کاهش میل جنسی
رالوکسیفن
- خطر لخته شدن خون، به ویژه در ریهها و پاها
- سکته مغزی در زیرگروههای خاص
سرکوب تخمدان
- از دست دادن استخوان
- نوسانات خلقی، افسردگی و از دست دادن میل جنسی
مهارکنندههای آروماتاز
- خطر حمله قلبی، آنژین صدری، نارسایی قلبی و کلسترول بالا
- از دست دادن استخوان
- درد مفاصل
- نوسانات خلقی و افسردگی
فولوسترانت
- علائم گوارشی، از جمله تهوع، استفراغ و یبوست
- ضعف و خستگی
- درد، از جمله درد استخوان، درد کمر، درد اسکلتی عضلانی ، درد مفاصل و درد در اندامها
- سردرد
- گرگرفتگی
- مشکلات تنفسی، از جمله تنفس دردناک، تنگی نفس و سرفه
- از دست دادن اشتها
آیا داروهای دیگر میتوانند با هورموندرمانی تداخل داشته باشند؟
برخی داروها، از جمله چندین داروی ضد افسردگی که معمولاً تجویز میشوند (آنهایی که در دسته مهارکنندههای انتخابی بازجذب سروتونین یا SSRIها قرار میگیرند)، آنزیمی به نام CYP2D6 را مهار میکنند. این آنزیم نقش مهمی در استفاده بدن از تاموکسیفن ایفا میکند، زیرا CYP2D6 تاموکسیفن را به مولکولها یا متابولیتهایی تجزیه میکند که بسیار فعالتر از خود تاموکسیفن هستند.
این احتمال که SSRIها ممکن است با مهار CYP2D6، متابولیسم تاموکسیفن را کند کرده و اثربخشی آن را کاهش دهند، با توجه به اینکه حدود یک چهارم بیماران مبتلا به سرطان پستان افسردگی بالینی را تجربه میکنند و ممکن است با SSRIها درمان شوند، نگرانکننده است. علاوه بر این، SSRIها گاهی اوقات برای درمان گرگرفتگی ناشی از هورموندرمانی استفاده میشوند.
بسیاری از متخصصان پیشنهاد میکنند بیمارانی که داروهای ضد افسردگی را همراه با تاموکسیفن مصرف میکنند، باید گزینههای درمانی را با پزشکان خود در میان بگذارند، مانند تغییر از یک SSRI که مهارکننده قوی CYP2D6 است، مانند پاروکستین هیدروکلراید (Paxil)، به یک مهارکننده ضعیفتر، مانند سرترالین (Zoloft) یا سیتالوپرام (Celexa)، یا به یک داروی ضد افسردگی که CYP2D6 را مهار نمیکند، مانند ونلافاکسین (Effexor) (31). یا پزشکان ممکن است به بیماران یائسه خود پیشنهاد دهند که به جای تاموکسیفن، یک مهارکننده آروماتاز مصرف کنند.
سایر داروهایی که CYP2D6 را مهار میکنند عبارتند از:
- کینیدین، که برای درمان ریتمهای غیرطبیعی قلب استفاده میشود
- دیفن هیدرامین ، که یک آنتیهیستامین است
- سایمتیدین، که برای کاهش اسید معده استفاده میشود
افرادی که تاموکسیفن برایشان تجویز میشود، باید در مورد مصرف سایر داروها با پزشک خود مشورت کنند.
منابع منتخب
- Kohler BA, Sherman RL, Howlader N, et al. Annual Report to the Nation on the Status of Cancer, 1975–2011, featuring incidence of breast cancer subtypes by race/ethnicity, poverty, and state. Journal of the National Cancer Institute 2015; 107(6):djv048. [PubMed Abstract]
- Joe BN. Clinical features, diagnosis, and staging of newly diagnosed breast cancer. In: UpToDate. Burstein HJ, Vora SR (eds.). Waltham, MA: UpToDate, 2019.
- Rudlowski C. Male breast cancer. Breast Care (Basel) 2008; 3(3):183–189. [PubMed Abstract]
- Early Breast Cancer Trialists’ Collaborative Group (EBCTCG), Davies C, Godwin J, et al. Relevance of breast cancer hormone receptors and other factors to the efficacy of adjuvant tamoxifen: Patient-level meta-analysis of randomised trials. Lancet 2011; 378(9793):771–784. [PubMed Abstract]
- Untch M, Thomssen C. Clinical practice decisions in endocrine therapy. Cancer Investigation 2010; 28 Suppl 1:4–13. [PubMed Abstract]
- Regan MM, Neven P, Giobbie-Hurder A, et al. Assessment of letrozole and tamoxifen alone and in sequence for postmenopausal women with steroid hormone receptor-positive breast cancer: The BIG 1–98 randomised clinical trial at 8.1 years median follow-up. Lancet Oncology 2011; 12(12):1101–1108. [PubMed Abstract]
- Burstein HJ, Griggs JJ. Adjuvant hormonal therapy for early-stage breast cancer. Surgical Oncology Clinics of North America 2010; 19(3):639–647. [PubMed Abstract]
- Early Breast Cancer Trialists’ Collaborative Group (EBCTCG). Aromatase inhibitors versus tamoxifen in early breast cancer: Patient-level meta-analysis of the randomised trials. Lancet 2015; 386(10001):1341–1352. [PubMed Abstract]
- Francis PA, Pagani O, Fleming GF, et al. Tailoring adjuvant endocrine therapy for premenopausal breast cancer. New England Journal of Medicine 2018; 379(2):122–137. [PubMed Abstract]
- Howell A, Pippen J, Elledge RM, et al. Fulvestrant versus anastrozole for the treatment of advanced breast carcinoma: A prospectively planned combined survival analysis of two multicenter trials. Cancer 2005; 104(2):236–239. [PubMed Abstract]
- Robertson JFR, Bondarenko IM, Trishkina E, et al. Fulvestrant 500 mg versus anastrozole 1 mg for hormone receptor-positive advanced breast cancer (FALCON): An international, randomised, double-blind, phase 3 trial. Lancet 2016; 388(10063):2997-3005. [PubMed Abstract]
- Cuzick J, Sestak I, Baum M, et al. Effect of anastrozole and tamoxifen as adjuvant treatment for early-stage breast cancer: 10-year analysis of the ATAC trial. Lancet Oncology 2010; 11(12):1135–1141. [PubMed Abstract]
- Mouridsen H, Gershanovich M, Sun Y, et al. Phase III study of letrozole versus tamoxifen as first-line therapy of advanced breast cancer in postmenopausal women: Analysis of survival and update of efficacy from the International Letrozole Breast Cancer Group. Journal of Clinical Oncology 2003; 21(11):2101–2109. [PubMed Abstract]
- Mauri D, Pavlidis N, Polyzos NP, Ioannidis JPA. Survival with aromatase inhibitors and inactivators versus standard hormonal therapy in advanced breast cancer: Meta-analysis. Journal of the National Cancer Institute 2006; 98(18):1285–1291. [PubMed Abstract]
- Finn RS, Martin M, Rugo HS, et al. Palbociclib and letrozole in advanced breast cancer. New England Journal of Medicine 2016; 375(20):1925–1936. [PubMed Abstract]
- Cristofanilli M, Turner NC, Bondarenko I, et al. Fulvestrant plus palbociclib versus fulvestrant plus placebo for treatment of hormone-receptor-positive, HER2-negative metastatic breast cancer that progressed on previous endocrine therapy (PALOMA-3): Final analysis of the multicentre, double-blind, phase 3 randomised controlled trial. Lancet Oncology 2016; 17(4):425–439. [PubMed Abstract]
- Sledge GW Jr, Toi M, Neven P, et al. MONARCH 2: Abemaciclib in combination with fulvestrant in women with HR+/HER2- advanced breast cancer who had progressed while receiving endocrine therapy. Journal of Clinical Oncology 2017; 35(25):2875–2884. [PubMed Abstract]
- Dickler MN, Tolaney SM, Rugo HS, et al. MONARCH 1, a phase II Study of abemaciclib, a CDK4 and CDK6 inhibitor, as a single agent, in patients with refractory HR+/HER2- metastatic breast cancer. Clinical Cancer Research 2017; 23(17):5218–5224. [PubMed Abstract]
- Tripathy D, Im SA, Colleoni M, et al. Ribociclib plus endocrine therapy for premenopausal women with hormone-receptor-positive, advanced breast cancer (MONALEESA-7): A randomised phase 3 trial. Lancet Oncology 2018; 19(7):904–915. [PubMed Abstract]
- Im SA, Lu YS, Bardia A, et al. Overall survival with ribociclib plus endocrine therapy in breast cancer. New England Journal of Medicine 2019; 381(4):307–316. [PubMed Abstract]
- Slamon DJ, Neven P, Chia S, et al. Phase III randomized study of ribociclib and fulvestrant in hormone receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer: MONALEESA-3. Journal of Clinical Oncology 2018; 36(24):2465–2472. [PubMed Abstract]
- André F, Ciruelos E, Rubovszky G, et al. Alpelisib for PIK3CA-mutated, hormone receptor-positive advanced breast cancer. New England Journal of Medicine 2019; 380(20):1929–1940. [PubMed Abstract]
- Rimawi M, Ferrero JM, de la Haba-Rodriguez J, et al. First-line trastuzumab plus an aromatase inhibitor, with or without pertuzumab, in human epidermal growth factor receptor 2-positive and hormone receptor-positive metastatic or locally advanced breast cancer (PERTAIN): A randomized, open-label phase II trial. Journal of Clinical Oncology 2018; 36(28):2826–2835. [PubMed Abstract]
- Chia YH, Ellis MJ, Ma CX. Neoadjuvant endocrine therapy in primary breast cancer: Indications and use as a research tool. British Journal of Cancer 2010; 103(6):759–764. [PubMed Abstract]
- Vogel VG, Costantino JP, Wickerham DL, et al. Effects of tamoxifen vs raloxifene on the risk of developing invasive breast cancer and other disease outcomes: The NSABP Study of Tamoxifen and Raloxifene (STAR) P–2 trial. JAMA 2006; 295(23):2727–2741. [PubMed Abstract]
- Cuzick J, Sestak I, Cawthorn S, et al. Tamoxifen for prevention of breast cancer: Extended long-term follow-up of the IBIS-I breast cancer prevention trial. Lancet Oncology 2015; 16(1):67–75. [PubMed Abstract]
- Vogel VG, Costantino JP, Wickerham DL, et al. Update of the National Surgical Adjuvant Breast and Bowel Project Study of Tamoxifen and Raloxifene (STAR) P-2 Trial: Preventing breast cancer. Cancer Prevention Research 2010; 3(6):696–706. [PubMed Abstract]
- Goss PE, Ingle JN, Alés-Martínez JE, et al. Exemestane for breast-cancer prevention in postmenopausal women. New England Journal of Medicine 2011; 364(25):2381–2391. [PubMed Abstract]
- Cuzick J, Sestak I, Forbes JF, et al. Anastrozole for prevention of breast cancer in high-risk postmenopausal women (IBIS-II): An international, double-blind, randomised placebo-controlled trial. Lancet 2014; 383(9922):1041–1048. [PubMed Abstract]
- Fisher B, Costantino JP, Wickerham DL, et al. Tamoxifen for prevention of breast cancer: Report of the National Surgical Adjuvant Breast and Bowel Project P–1 Study. Journal of the National Cancer Institute 1998; 90(18):1371–1388. [PubMed Abstract]
- Hemeryck A, Belpaire FM. Selective serotonin reuptake inhibitors and cytochrome P-450 mediated drug–drug interactions: An update. Current Drug Metabolism 2002; 3(1):13–37. [PubMed Abstract]
تهیه و تنظیم: سید طه نوربخش
تأیید و نظارت: فائزه محمدهاشم-متخصص ژنتیک