آنچه در این مطلب خواهید خواند
- آزمایش ژنتیک برای بررسی خطر ابتلا به سرطان ارثی چیست؟
- آزمایش ژنتیک چگونه انجام میشود؟
- چه کسانی باید آزمایش ژنتیک برای بررسی خطر ابتلا به سرطان ارثی را در نظر بگیرند؟
- چه آزمایشهای ژنتیکی برای بررسی خطر ابتلا به سرطان ارثی در دسترس است؟
- نتایج آزمایش ژنتیک چه معنایی دارند؟
- چه زمانی باید آزمایش ژنتیک مکرر در نظر گرفته شود؟
- نقش مشاوره ژنتیک در آزمایش ژنتیک برای بررسی خطر ابتلا به سرطان ارثی چیست؟
- پیامدهای سلامتی نتایج آزمایش ژنتیک برای خویشاوندان خونی چیست؟
- مزایا و معایب آزمایش ژنتیک برای تعیین خطر سرطان چیست؟
- چه کسی به نتایج آزمایش ژنتیک یک فرد دسترسی دارد؟
- آیا میتوان از آزمایشهای ژنتیکی خانگی یا مستقیم به مصرفکننده (DTC) برای بررسی خطر سرطان استفاده کرد؟
- آزمایشگاههای آزمایش ژنتیک چگونه تنظیم میشوند؟
- چه تحقیقاتی برای بهبود آزمایش ژنتیک برای خطر ابتلا به سرطان ارثی انجام میشود؟
آزمایش ژنتیک برای بررسی خطر ابتلا به سرطان ارثی چیست؟
آزمایش ژنتیک به دنبال تغییرات ارثی خاص (که گاهی اوقات جهش یا واریانتهای بیماریزا نامیده میشوند) در ژنهای فرد میگردد که ممکن است خطر ابتلا به بیماریهایی مانند سرطان را افزایش دهد. تصور میشود حدود ۵ تا ۱۰ درصد از کل سرطانها ناشی از تغییرات ژنتیکی مضری هستند که از والدین به ارث میرسند.
گاهی اوقات، حتی اگر تغییر ژنتیکی مضر ارثی در خانواده وجود نداشته باشد، سرطان میتواند در خانوادهها ارثی باشد. به عنوان مثال، یک محیط یا رفتار مشترک، مانند مصرف دخانیات، میتواند باعث ایجاد سرطانهای مشابه در بین اعضای خانواده شود. با این حال، الگوهای خاصی که در اعضای یک خانواده مشاهده میشود – مانند انواع سرطانهایی که ایجاد میشوند، سایر بیماریهای غیر سرطانی که مشاهده میشوند و سنینی که معمولاً سرطان در آنها ایجاد میشود – ممکن است نشاندهنده وجود یک تغییر ژنتیکی مضر ارثی باشد که خطر ابتلا به سرطان را افزایش میدهد.
ژنهای زیادی که تغییرات ژنتیکی مضر در آنها خطر ابتلا به سرطان را افزایش میدهد، شناسایی شدهاند. داشتن یک تغییر ژنتیکی مضر ارثی در یکی از این ژنها گاهی اوقات به عنوان سندرم سرطان ارثی شناخته میشود. آزمایش ژنتیک خون یا بزاق میتواند برای شناسایی اینکه آیا کسی تغییر ژنتیکی مضر ارثی در یکی از این ژنها دارد یا خیر، استفاده شود.
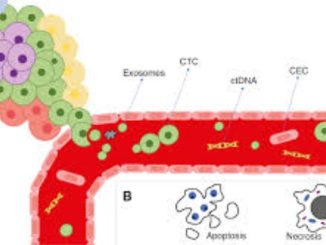
آزمایش ژنتیک برای خطر ابتلا به سرطان ارثی با آزمایش ژنتیک تومورها که گاهی اوقات برای هدایت درمان استفاده میشود، متفاوت است. آزمایش ژنتیک تومور، که ممکن است به عنوان تعیین توالی DNA تومور، آزمایش سوماتیک یا آزمایش نشانگر زیستی نیز شناخته شود، به دنبال تغییرات ژنتیکی است که در طول زندگی فرد رخ داده است. گاهی اوقات میتواند تغییرات ارثی را نیز تشخیص دهد، اما جایگزین آزمایش برای خطر ابتلا به سرطان ارثی نمیشود.
آزمایش ژنتیک چگونه انجام میشود؟
آزمایشهای ژنتیکی معمولاً توسط یک مشاور ژنتیک ، پزشک یا سایر ارائه دهندگان خدمات درمانی که سابقه پزشکی شخصی و خانوادگی فرد را بررسی کرده و یک الگوی سرطان ارثی بالقوه را شناسایی کردهاند، درخواست میشوند.
آزمایش روی نمونه کوچکی از مایعات یا بافت بدن – معمولاً خون، اما گاهی بزاق، سلولهای داخل گونه یا سلولهای پوست – انجام میشود. سپس نمونه به آزمایشگاه آزمایش ژنتیک ارسال میشود. نتایج آزمایش معمولاً حدود ۲ تا ۳ هفته بعد آماده میشوند.
بیمه سلامت معمولاً مشاوره ژنتیک و آزمایشهای ژنتیکی که از نظر پزشکی ضروری تلقی میشوند را پوشش میدهد. افراد فاقد بیمه میتوانند از طریق سازمانهایی که برنامههای یارانهای ارائه میدهند، به آزمایش ژنتیک مقرونبهصرفه دسترسی پیدا کنند.
چه کسانی باید آزمایش ژنتیک برای بررسی خطر ابتلا به سرطان ارثی را در نظر بگیرند؟
دستورالعملهای بالینی، آزمایش ژنتیک را برای هر کسی که قبل از ۵۰ سالگی به سرطان پستان سهگانه منفی، سرطان تخمدان، سرطان پانکراس، سرطان روده بزرگ، سرطان پروستات متاستاتیک یا سرطان پستان مردان مبتلا شده است، توصیه میکنند. برای افراد مبتلا به این سرطانها، دانستن اینکه آیا سرطان آنها مربوط به یک تغییر ژنتیکی مضر ارثی است یا خیر، میتواند به انتخاب درمان بهینه برای آنها کمک کند. این اطلاعات همچنین ممکن است برای بستگان خونی آنها نیز مفید باشد.
به طور کلی توصیه میشود افرادی که سابقه پزشکی شخصی یا خانوادگی خاصی دارند که احتمال ابتلا به سندرم سرطان ارثی را نشان میدهد، با پزشک یا مشاور ژنتیک خود مشورت کنند تا ببینند آیا آزمایش ژنتیک برای آنها مناسب است یا خیر. ویژگیهایی که احتمال ابتلا به سندرم ژنتیکی ارثی را نشان میدهند عبارتند از:
- عضوی از خانواده که دچار تغییر ژنتیکی مضر ارثی شناختهشدهای است که خطر ابتلا به سرطان را افزایش میدهد
- سرطان در سنین جوانی تشخیص داده شده است (برای مثال، سرطان روده بزرگ قبل از ۵۰ سالگی تشخیص داده شده است)
- چندین نوع مختلف سرطان در یک فرد رخ داده است
- سرطان در چندین عضو خانواده تشخیص داده شده است، به خصوص با الگوهایی مانند
- چندین نفر از بستگان درجه یک (والدین، خواهر و برادر یا فرزندان یک فرد) مبتلا به همان نوع سرطان هستند
- اعضای خانواده مبتلا به سرطان پستان یا تخمدان
- اعضای خانواده مبتلا به سرطان روده بزرگ و سرطان آندومتر
- سرطان در هر دو اندام در مجموعهای از اندامهای جفت، مانند هر دو کلیه یا هر دو پستان
- انواع نادر سرطان (به عنوان مثال، سرطان پستان مردان)
- وجود نقایص مادرزادی که با سندرمهای سرطان ارثی مرتبط هستند، مانند برخی بیماریهای غیرسرطانی یا ناهنجاریهای جسمی
- عضویت در یک گروه نژادی یا قومی که خطر ابتلا به یک سندرم استعداد ابتلا به سرطان ارثی در آن افزایش یافته است و همچنین داشتن یک یا چند مورد از ویژگیهای فوق
به طور کلی توصیه میشود که در صورت امکان، مشاوره ژنتیک و آزمایش برای سندرم سرطان ارثی با یکی از اعضای خانواده که مبتلا به سرطان بوده است، آغاز شود.
چه آزمایشهای ژنتیکی برای بررسی خطر ابتلا به سرطان ارثی در دسترس است؟
انواع مختلفی از آزمایشهای ژنتیکی وجود دارد که برای جستجوی تغییرات ژنی ارثی مضر که ممکن است در یک خانواده وجود داشته باشد، استفاده میشوند. رویکرد استاندارد از آزمایشهایی استفاده میکند که به طور همزمان واریانتهای مضر را در چندین ژن جستجو میکنند. این آزمایشها که آزمایشهای چند ژنی (یا پنلی) نامیده میشوند، اغلب زمانی استفاده میشوند که جهش ژنی شناخته شدهای در یک خانواده وجود نداشته باشد. بسته به سابقه شخصی و خانوادگی بیمار و همچنین ترجیح آنها برای میزان اطلاعاتی که میخواهند، ارائه دهنده خدمات درمانی ممکن است یک آزمایش پنلی را که بر ژنهای نوع خاصی از سرطان تمرکز دارد، یا ممکن است یک آزمایش پنلی گسترده را که ژنهای مرتبط با انواع سرطانهای رایج را بررسی میکند، سفارش دهد.
وقتی وجود یک واریانت ژنی در خانواده مشخص میشود، گاهی اوقات کل ژن برای بررسی تغییرات آزمایش میشود. از طرف دیگر، آزمایش ممکن است فقط بر واریانت خاصی که وجود آن در خانواده شناخته شده است، تمرکز کند.

نتایج آزمایش ژنتیک چه معنایی دارند؟
آزمایش ژنتیک میتواند چندین نتیجه ممکن ارائه دهد: مثبت، منفی، منفی واقعی، منفی بدون اطلاعات مفید، یا نوعی با اهمیت نامشخص (VUS).
نتیجه مثبت. نتیجه مثبت آزمایش به این معنی است که آزمایشگاه یک تغییر ژنتیکی را پیدا کرده است که با افزایش خطر ابتلا به سرطان مرتبط است. چنین تغییرات ژنتیکی مضر، واریانتهای بیماریزا یا احتمالاً بیماریزا نامیده میشوند. نتیجه مثبت ممکن است:
- برای فردی که سرطان دارد، تأیید شود که سرطان احتمالاً به دلیل یک تغییر ژنتیکی ارثی بوده است و به طور بالقوه به انتخاب درمان کمک میکند.
- افزایش خطر ابتلا به سرطان(های) خاص در آینده را نشان میدهد و مدیریت آینده را برای کاهش این خطر راهنمایی میکند، از جمله:
- معاینه در سنین پایینتر یا دفعات بیشتر برای بررسی علائم سرطان
- مصرف دارو یا انجام جراحی برای کاهش خطر ابتلا به سرطان
- تغییر رفتارهای شخصی (مانند ترک سیگار، ورزش بیشتر و داشتن رژیم غذایی سالمتر) برای کاهش خطر ابتلا به برخی سرطانها
- دریافت کمک برای هدایت تصمیمات در مورد باروری و بارداری
- اطلاعات مهمی ارائه دهید که میتواند به سایر اعضای خانواده در تصمیمگیری در مورد مراقبتهای بهداشتی خود کمک کند، مانند اینکه آیا آزمایش ژنتیک انجام دهند تا ببینند آیا آنها نیز تغییر ژنتیکی مضر را به ارث بردهاند یا خیر.
نتیجه منفی. نتیجه آزمایش منفی به این معنی است که آزمایشگاه هیچ تغییر ژنتیکی مضری در ژنهای آزمایش شده با فناوری موجود پیدا نکرده است. این نتیجه زمانی بیشترین کاربرد را دارد که یک واریانت خاص بیماریزا در یک خانواده وجود داشته باشد. در چنین حالتی، یک نتیجه منفی میتواند نشان دهد که عضو آزمایش شده خانواده، واریانت موجود در خانواده خود را به ارث نبرده است. چنین نتیجه آزمایشی، منفی واقعی نامیده میشود. نتیجه منفی واقعی به این معنی نیست که هیچ خطری برای سرطان وجود ندارد، بلکه به این معنی است که خطر احتمالاً مشابه خطر ابتلا به سرطان در یک فرد در جمعیت عمومی است.
وقتی فردی سابقه خانوادگی قوی سرطان دارد اما هیچ تغییر ژنتیکی مضری که با آن سرطان مرتبط باشد در خانوادهاش یافت نشده باشد، نتیجه آزمایش منفی به عنوان منفی بیاطلاع (uninformative) طبقهبندی میشود. ممکن است خانواده هنوز یک واریانت ژنی شناسایی نشده داشته باشند که منجر به افزایش خطر ابتلا به سرطان شود. با تحقیقات بیشتر و پیشرفتهای فناوری، این امکان وجود دارد که آزمایشهای ژنتیکی اضافی در آینده یک تغییر ژنتیکی مضر را شناسایی کنند.
در صورت منفی بودن نتیجه آزمایش، مهم است که پزشکان و مشاوران ژنتیک فرد اطمینان حاصل کنند که فرد بر اساس سابقه شخصی و خانوادگی و سایر عوامل خطری که ممکن است داشته باشد، پیگیری پزشکی مناسبی را دریافت میکند. حتی زمانی که آزمایش ژنتیک منفی است، برخی از افراد ممکن است از معاینات مکرر – به ویژه در مورد منفی بودن بدون اطلاعات – بهرهمند شوند.
واریانت با اهمیت نامشخص. واریانت با اهمیت نامشخص (VUS) یک تغییر ژنتیکی است که دادههای کافی برای دانستن اینکه آیا خطر ابتلا به سرطان را افزایش میدهد یا خیر، در دسترس نیست. یک VUS ممکن است در آینده با کسب اطلاعات بیشتر محققان در مورد این تغییرات ژنتیکی، دوباره طبقهبندی شود. اغلب، یک VUS به عنوان خوشخیم (که خطر ابتلا به سرطان را افزایش نمیدهد) طبقهبندی میشود، بنابراین این نتیجه معمولاً در تصمیمگیریهای مراقبتهای بهداشتی در نظر گرفته نمیشود.
گاهی اوقات ممکن است در نهایت مشخص شود که یک VUS با افزایش خطر ابتلا به سرطان مرتبط است. بنابراین، مهم است که فردی که نتیجه VUS دارد، با ارائه دهنده آزمایش که آزمایش را انجام داده است، در تماس باشد تا اطمینان حاصل شود که از هرگونه اطلاعات جدید در مورد واریانت ژنی مطلع خواهد شد.
چه زمانی باید آزمایش ژنتیک مکرر در نظر گرفته شود؟
ساختار ژنتیکی یک فرد با گذشت زمان تغییر نمیکند، بنابراین معمولاً نیازی به تکرار یک آزمایش ژنتیکی خاص نیست. با این حال، در شرایط خاص، آزمایش ژنتیکی بیشتر ممکن است مناسب باشد:
- پس از یک نتیجه منفی غیرموثق، آزمایشهای آینده ممکن است یک وارذمضر را که در زمان آزمایش اصلی شناخته نشده بود، نشان دهند. ژنهای کاندید جدید به طور منظم کشف میشوند و پیشرفتهای مداوم در فناوری آزمایش ممکن است پزشکان را قادر سازد واریانتهایی که در ژنهای شناخته شده در ایجاد سرطان، قبلاً غیرقابل تشخیص بودند، را شناسایی کنند.
- گاهی اوقات، ممکن است برای تأیید نتیجهی نامشخص یافتشده در خون یا بزاق، تکرار آزمایش ژنتیکی روی نوع بافت دوم (مثلاً بیوپسی پوست) مورد نیاز باشد.
- وقتی یک ویژگی بالینی یا سرطان جدید رخ میدهد که احتمال وجود یک واریانت ارثی در ژنی را که در آزمایش اصلی لحاظ نشده بود، مطرح میکند، آزمایش ژنهای اضافی ممکن است مناسب باشد.
نقش مشاوره ژنتیک در آزمایش ژنتیک برای بررسی خطر ابتلا به سرطان ارثی چیست؟
مشاوره ژنتیک معمولاً قبل از هرگونه آزمایش ژنتیکی برای بررسی خطر ابتلا به سرطان ارثی توصیه میشود. همچنین ممکن است پس از آزمایش نیز انجام شود، به خصوص اگر نتیجه مثبت باشد و فرد نیاز به کسب اطلاعات بیشتر در مورد معنای این نتیجه برای خود داشته باشد. این مشاوره باید توسط یک مشاور ژنتیک آموزش دیده یا سایر متخصصان مراقبتهای بهداشتی که در ژنتیک سرطان تجربه دارند، انجام شود.
مشاوره ژنتیک معمولاً جنبههای زیادی از فرآیند آزمایش را پوشش میدهد، از جمله:
- ارزیابی احتمال وجود خطر ارثی سرطان در خانواده
- بحث در مورد:
- مناسب بودن آزمایش ژنتیک و مضرات و مزایای بالقوه آزمایش
- پیامدهای پزشکی نتایج آزمایش مثبت، منفی و نامشخص
- خطرات و مزایای روانشناختی اطلاع از نتایج آزمایش ژنتیک
- خطر انتقال یک نوع به کودکان
- تأثیر آزمایش برای خانواده
- گزینههای آزمایش ژنتیکی که بر اساس سابقه شخصی و خانوادگی مناسبترین گزینهها هستند
- توضیح آزمایش (آزمایشهای) خاصی که ممکن است مورد استفاده قرار گیرند و دقت فنی آزمایش (آزمایشها) و تفسیر آنها
مشاوره ژنتیک همچنین ممکن است شامل بحث در مورد توصیههایی برای استراتژیهای کاهش خطر و رویکردهای غربالگری پیشرفته، ارجاع به گروههای حمایتی و سایر منابع اطلاعاتی و حمایت عاطفی از فردی که نتایج را دریافت میکند، باشد.
قبل از درخواست آزمایش ژنتیک، رضایت کتبی آگاهانه اخذ میشود. افراد با امضای فرمی که تأیید میکند در مورد هدف آزمایش، پیامدهای پزشکی آن، خطرات و مزایای آن، جایگزینهای احتمالی آزمایش و حقوق حریم خصوصی خود به آنها اطلاع داده شده و آنها را درک کردهاند، رضایت خود را اعلام میکنند.
پیامدهای سلامتی نتایج آزمایش ژنتیک برای خویشاوندان خونی چیست؟
برخلاف اکثر آزمایشهای پزشکی دیگر، آزمایشهای ژنتیکی میتوانند نه تنها اطلاعاتی در مورد فرد مورد آزمایش، بلکه در مورد خویشاوندان خونی آن فرد نیز آشکار کنند. اعضای خانواده ممکن است در مورد اینکه آیا میخواهند بدانند که آیا تغییر ارثی دارند که خطر ابتلا به سرطان را در آنها افزایش میدهد یا خیر، نظرات متفاوتی داشته باشند.
گفتگو با یک مشاور ژنتیک میتواند به اعضای خانواده فردی که آزمایش ژنتیک او مثبت بوده است، کمک کند تا در مورد گزینههای آزمایش ژنتیک خود اطلاعات کسب کنند و در صورت اطلاع از وجود یک تغییر ژنتیکی که آنها را در معرض خطر ابتلا به سرطان قرار میدهد، گزینههایی را که ممکن است با آن مواجه شوند، بهتر درک کنند.

مزایا و معایب آزمایش ژنتیک برای تعیین خطر سرطان چیست؟
صرف نظر از نتایج، آزمایش ژنتیک مزایایی دارد.
- اگر آزمایش نشان دهد که فرد تغییر ژنتیکی مضر شناساییشده در خانواده را به ارث نبرده است (نتیجه منفی آموزنده یا واقعی)، میتواند آرامش خاطر ایجاد کند.
- آزمایشی که وجود تغییرات مضر در تمام ژنهای شناختهشدهی سرطان را رد میکند، به فرد اجازه میدهد تا خطر ابتلا به سرطان خود را بر اساس سابقهی شخصی و خانوادگیاش مدیریت کند.
- آزمایشی که یک تغییر ژنتیکی مضر (نتیجه مثبت آزمایش) را شناسایی میکند، به فرد فرصتی میدهد تا خطر ابتلا به سرطان خود را درک کند و در برخی موارد، به طور بالقوه آن را مدیریت کند.
- برای افرادی که قبلاً به سرطان مبتلا شدهاند، نتایج آزمایش ژنتیک میتواند به پیشنهاد مناسبترین درمانها کمک کند و اطلاعاتی در مورد خطر ابتلا به سایر سرطانها ارائه دهد.
- آزمایش ژنتیک فرصتی را برای اعضای خانواده فراهم میکند تا از خطر ابتلا به سرطان خود مطلع شوند.
معایب احتمالی آزمایش ژنتیک عبارتند از:
- استرس روانی ناشی از آگاهی از اینکه فرد دچار تغییر ژنتیکی شده است که نه تنها خطر ابتلا به سرطان را در خود او، بلکه در بستگان خونی او، از جمله فرزندان، نیز افزایش میدهد (که گاهی اوقات «گناه والدین» نامیده میشود)
- احساس «گناه بازمانده» پس از فهمیدن اینکه تغییر مضری که در سایر اعضای خانواده وجود دارد، در فرد وجود ندارد.
- عدم اطمینان و استرس ناشی از دریافت نتیجه آزمایش بیاطلاع، مانند گزارش یک نوع با اهمیت نامشخص (VUS)
- هزینه آزمایش ژنتیک، در صورت عدم پوشش بیمه
- نیاز به پیگیری پزشکی و اقدامات پیشگیرانه بالقوه پرهزینه و زمانبر در صورت مثبت بودن آزمایش
- مسائل مربوط به حریم خصوصی و تبعیض
- احتمال نتیجه مثبت کاذب نادر (منجر به پیگیری غیرضروری و استرس روانی) یا نتیجه منفی کاذب (منجر به احساس اشتباه کاهش خطر سرطان)
- احتمال اقدام فرد بر اساس اطلاعات نادرست، ناقص یا گمراهکننده، در صورتی که نتایج آزمایش به طور مناسب برای او توضیح داده نشود.
چه کسی به نتایج آزمایش ژنتیک یک فرد دسترسی دارد؟
نتایج آزمایشهای پزشکی معمولاً در پرونده پزشکی فرد ثبت میشوند، به خصوص اگر پزشک یا سایر ارائهدهندگان خدمات درمانی، آزمایش را تجویز کرده باشند یا در مورد نتایج آزمایش با آنها مشورت شده باشد. بنابراین، افرادی که آزمایش ژنتیک را در نظر میگیرند باید درک کنند که نتایج آنها ممکن است برای دیگران که دسترسی قانونی و مشروع به پرونده پزشکی آنها دارند، آشکار شود.
به طور کلی، نتایج ژنتیکی و اطلاعات موجود در پرونده پزشکی یک فرد تحت پوشش قانون حفظ حریم خصوصی قانون قابلیت انتقال و پاسخگویی اطلاعات سلامت (HIPAA) مصوب سال ۱۹۹۶ قرار دارد. قانون حفظ حریم خصوصی HIPAA ایجاب میکند که ارائه دهندگان مراقبتهای بهداشتی و سایر افراد دارای دسترسی به پرونده پزشکی، با تعیین محدودیتهایی در مورد استفاده و افشای این اطلاعات، از اطلاعات سلامت قابل شناسایی فرد محافظت کنند. همچنین به افراد این اختیار را میدهد که برخی از کاربردها و اشتراکگذاری اطلاعات مرتبط با سلامت خود را کنترل کنند. معمولاً این بدان معناست که اگر فرد یا سازمانی که در مراقبتهای پزشکی او دخیل نیست، بخواهد به پرونده پزشکی او دسترسی پیدا کند، ابتدا باید اجازه دهد. بسیاری از ایالتها نیز قوانینی برای محافظت از حریم خصوصی بیمار و محدود کردن انتشار اطلاعات ژنتیکی و سایر اطلاعات سلامت دارند.
علاوه بر این، حتی اگر نتایج آزمایش ژنتیک قابل دسترسی یا شناخته شده باشند، حمایتهای قانونی برای جلوگیری از تبعیض ژنتیکی وجود دارد؛ این امر میتواند در صورتی رخ دهد که شرکتهای بیمه درمانی یا کارفرمایان به دلیل داشتن تغییر ژنی که خطر ابتلا به بیماریهایی مانند سرطان را افزایش میدهد، یا به دلیل داشتن سابقه خانوادگی قوی از بیماریهایی مانند سرطان، با افراد متفاوت رفتار کنند.
قانون عدم تبعیض اطلاعات ژنتیکی (GINA)، که در سال ۲۰۰۸ به قانون تبدیل شد، تبعیض بر اساس اطلاعات ژنتیکی را در تعیین واجد شرایط بودن برای بیمه سلامت یا نرخها و مناسب بودن برای اشتغال ممنوع میکند. با این حال، GINA اعضای ارتش را پوشش نمیدهد و در مورد بیمه عمر، بیمه معلولیت یا بیمه مراقبت طولانی مدت اعمال نمیشود. برخی ایالتها قوانین عدم تبعیض ژنتیکی اضافی دارند که احتمال تبعیض در این زمینهها را بررسی میکند.
آیا میتوان از آزمایشهای ژنتیکی خانگی یا مستقیم به مصرفکننده (DTC) برای بررسی خطر سرطان استفاده کرد؟
تعداد فزایندهای از شرکتها، برخلاف آزمایش ژنتیکی که توسط ارائهدهنده خدمات درمانی در محیط بالینی تجویز میشود، آزمایش ژنتیک در منزل ارائه میدهند. افراد خودشان نمونه بزاق یا سواب دهان را جمعآوری کرده و از طریق پست ارسال میکنند. شرکتها نتایج آزمایش را به روشهای مختلفی گزارش میدهند، اما اکثر آنها نتایج را در یک وبسایت امن ارائه میدهند یا گزارش را از طریق پست ارسال میکنند.
دو دسته کلی از آزمایشهای خانگی وجود دارد: آزمایش مستقیم به مصرفکننده و آزمایش ژنتیکی تحت هدایت مصرفکننده (که گاهی اوقات به عنوان آزمایش ژنتیکی مبتنی بر بیمار، دسترسی مستقیم یا آزمایش ژنتیکی با واسطه ارائهدهنده خدمات درمانی شناخته میشود).
آزمایشهای ژنتیکی مستقیم به مصرفکننده (DTC). اینها آزمایشهای ژنتیکی هستند که مشتریان میتوانند بدون دستور پزشک، خودشان سفارش دهند. افراد اغلب از آزمایشهای DTC برای بررسی تبار، کسب اطلاعات در مورد ویژگیهای شخصی مانند بیزاری از گشنیز و کسب اطلاعات در مورد سلامت (مانند پیشبینی خطر بیماری) استفاده میکنند. با این حال، این آزمایشها اطلاعات کامل سلامت ژنتیکی را ارائه نمیدهند و در بیشتر موارد، اطلاعاتی که ارائه میدهند برای استفاده در تصمیمگیریهای سلامت در نظر گرفته نشده است (یعنی از نظر بالینی قابل اجرا نیستند).
آزمایشهای ژنتیکی DTC که بهطور خاص برای واریانتهایی هستند که خطر ابتلا به سرطان بالایی دارند و از نظر بالینی قابل اجرا هستند، باید قبل از عرضه به بازار، توسط سازمان غذا و داروی آمریکا (FDA) تأیید شوند. از ژانویه 2024، تنها آزمایش ژنتیکی DTC مورد تأیید FDA برای آزمایشهای خطر ارثی سرطان، برای سه واریانت مختلف ژن BRCA است که در افراد با تبار یهودی اشکنازی رایج است. با این حال، صدها واریانت ژن BRCA وجود دارد که میتوانند خطر ابتلا به سرطان را در یک فرد و خانواده افزایش دهند، بنابراین نتیجه منفی BRCA در آزمایش DTC در اکثر افراد آموزنده نیست. حدود 80٪ از واریانتهای BRCA ایجادکننده سرطان با این رویکرد از دست میروند.
بسیاری از آزمایشهای DTC تبلیغ میکنند که میتوانند نتایج جالب و متنوعی از سلامت ارائه دهند یا دادههای ژنتیکی خام فرد را در اختیار قرار میدهند که میتوان از آنها برای ارزیابی انواع مختلف واریانتهای ژنومی استفاده کرد. با این حال، نگرانیهایی در مورد ادعاهای مطرح شده و شیوههای مورد استفاده برخی از این شرکتها مطرح شده است و ابزارهای آنلاینی که میتوانند برای تجزیه و تحلیل و تفسیر دادههای خام استفاده شوند، مستعد نادرستی هستند.
آزمایش ژنتیکی تحت هدایت مصرفکننده. این آزمایشها توسط مصرفکننده آغاز میشوند اما در نهایت توسط یک پزشک – یا پزشک خود فرد یا پزشکی که شرکت آزمایشکننده شناسایی میکند – سفارش داده میشوند. پزشکانی که توسط یک شرکت آزمایشکننده شناسایی میشوند، ممکن است انگیزهای برای سفارش آزمایش برند شرکت داشته باشند، چه بهترین آزمایش برای بیمار باشد چه نباشد. این پزشکان با بیماران ملاقات نمیکنند و ممکن است تمام اطلاعات لازم برای ارائه راهنمایی در مورد بهترین گزینههای آزمایش برای بیمار را نداشته باشند.
اگرچه آزمایشهای مورد استفاده در آزمایشهای مصرفکننده محور مشابه آزمایشهایی هستند که توسط پزشک متخصص در محیط بالینی تجویز میشوند، اما افرادی که آزمایش مصرفکننده محور را در نظر میگیرند باید توجه داشته باشند که آزمایشهای درخواستی ممکن است ژنهای بیشتری را نسبت به آنچه از نظر بالینی لازم است، بررسی کنند و این امر احتمال نتایج مثبت غیرمنتظره و اضطرابآور و یافتههای مربوط به متغیرهای با اهمیت نامشخص را افزایش میدهد. اکثر شرکتهایی که آزمایش ژنتیکی مصرفکننده محور ارائه میدهند، مشاوره ژنتیکی ارائه میدهند. با این حال، اگر کسی مشاوره را انتخاب نکند، ممکن است فرصتی برای بررسی نتایج خود با یک متخصص مراقبتهای بهداشتی نداشته باشد. بدون راهنمایی در مورد اینکه با توجه به سابقه شخصی و خانوادگی یا پیامدهای نتایج، کدام آزمایش ژنتیکی برای آنها مناسبتر است، افرادی که آزمایشهای ژنتیکی خانگی انجام میدهند، ممکن است دچار اضطراب بیمورد یا اطمینان خاطر کاذب شوند یا ممکن است بر اساس اطلاعات ناقص، تصمیمات مهمی در مورد درمان یا مراقبت پزشکی بگیرند.
آزمایش ژنتیک DTC و آزمایش ژنتیک به ابتکار مصرفکننده، هر دو با افزایش خطر تفسیر نادرست اطلاعات همراه هستند. به عنوان مثال، ممکن است فردی نتیجه آزمایش ژنتیک منفی داشته باشد و نداند که هنوز در معرض خطر بالای بیماری است و بر اساس سابقه خانوادگی خود واجد شرایط نظارت بیشتر باشد. برخی از شرکتهای بیمه ممکن است فقط هزینه مقدار یا نوع خاصی از آزمایش ژنتیک را پرداخت کنند، بنابراین اگر افراد از بیمه برای پرداخت هزینه آزمایش DTC استفاده کنند، ممکن است متوجه شوند که آزمایشهای بعدی که پزشکشان دستور داده است، تحت پوشش قرار نمیگیرند.
حریم خصوصی نتایج آزمایش ژنتیک در منزل به سیاستهای هر شرکت بستگی دارد. سیاستهای افشای اطلاعات شرکتها همیشه ارائه نمیشوند، یا ممکن است یافتن و درک آنها دشوار باشد. علاوه بر این، شرکتهایی که آزمایش در منزل ارائه میدهند ممکن است مشمول قوانین و مقررات حفظ حریم خصوصی فدرال و ایالتی که از اطلاعات ژنتیکی و سایر اطلاعات سلامت محافظت میکنند (مثلاً قانون حفظ حریم خصوصی HIPAA) نباشند. افرادی که آزمایش ژنتیک مبتنی بر مصرفکننده در منزل را در نظر میگیرند، باید قبل از ارسال نمونه، مطمئن شوند که سیاست حفظ حریم خصوصی و شرایط استفاده شرکت را درک میکنند.
سازمان غذا و داروی آمریکا (FDA) صفحهای در مورد آزمایشهای DTC دارد که اطلاعاتی در مورد نحوه تنظیم این آزمایشها ارائه میدهد. در سال 2024، FDA اعلام کرد که شروع به تنظیم آزمایشهای توسعهیافته در آزمایشگاه خواهد کرد، که شامل بسیاری از آزمایشهای مورد استفاده در آزمایشهای ژنتیکی تحت هدایت مصرفکننده میشود.
MedlinePlus، یک وبسایت سلامت مصرفکننده از کتابخانه ملی پزشکی در مؤسسات ملی بهداشت، اطلاعاتی در مورد آزمایش ژنتیک DTC دارد.
آزمایشگاههای آزمایش ژنتیک چگونه تنظیم میشوند؟
آزمایشگاههای ایالات متحده که آزمایشهای مرتبط با سلامت، از جمله آزمایشهای ژنتیکی، انجام میدهند، تحت برنامه اصلاحیههای بهبود آزمایشگاه بالینی (CLIA) تنظیم میشوند. آزمایشگاههایی که تحت CLIA گواهی دریافت میکنند، ملزم به رعایت استانداردهای فدرال برای کیفیت، دقت و قابلیت اطمینان آزمایشها هستند. همه آزمایشگاههایی که آزمایش ژنتیک انجام میدهند و نتایج را به اشتراک میگذارند، باید دارای گواهینامه CLIA باشند. با این حال، گواهینامه CLIA فقط نشان میدهد که استانداردهای مناسب کنترل کیفیت آزمایشگاه رعایت میشود. این گواهینامه تضمین نمیکند که آزمایش ژنتیکی انجام شده توسط یک آزمایشگاه از نظر پزشکی مفید یا به درستی تفسیر شود. علاوه بر این، آزمایشگاههای آزمایش ژنتیک مستقیم به مصرفکننده ملزم به رعایت CLIA نیستند، اما میتوانند این کار را انجام دهند. موسسه ملی تحقیقات ژنوم انسانی اطلاعات بیشتری را در صفحه تنظیم آزمایشهای ژنتیک خود در دسترس دارد.
چه تحقیقاتی برای بهبود آزمایش ژنتیک برای خطر ابتلا به سرطان ارثی انجام میشود؟
تحقیقات برای یافتن راههای بهتر برای تشخیص، درمان و پیشگیری از سرطان در افرادی که حامل واریانتهای ژنتیکی هستند که خطر ابتلا به برخی سرطانها را افزایش میدهند، ادامه دارد. دانشمندان همچنین در حال انجام مطالعاتی برای شناسایی تغییرات ژنتیکی جدیدی هستند که میتوانند خطر ابتلا به سرطان را در فرد افزایش دهند. همچنین کارهای زیادی برای افزایش دقت و ثبات طبقهبندی واریانتهای ژنتیکی شناسایی شده توسط آزمایش در حال انجام است.
هدف از یک مسیر تحقیقاتی دیگر، ارائه اطلاعات بهتر به پزشکان و بیماران در مورد خطرات واقعی سرطان مرتبط با واریانتهای ژنتیکی خاص، به ویژه واریانتهایی با اهمیت نامشخص است.
اگرچه دستورالعملهای طبابت بالینی توصیه میکنند که همه افراد مبتلا به سرطانهای خاص، آزمایش تغییر ژنتیکی ارثی انجام دهند، اما تنها درصد کمی از آنها آزمایش میدهند. احتمالاً عواملی که در پایین بودن میزان آزمایش نقش دارند، شامل دسترسی محدود به مشاوران ژنتیک و عدم اطمینان یا بیاعتمادی به آزمایش ژنتیک است.
منابع منتخب
- Chokoshvili D, Vears DF, Borry P. Growing complexity of (expanded) carrier screening: Direct-to-consumer, physician-mediated, and clinic-based offers. Best Practice & Research Clinical Obstetrics & Gynaecology 2017; 44: 57–67. [PubMed Abstract]
- Daly MB, Pal T, Maxwell KN, et al. NCCN Guidelines® Insights: Genetic/Familial High-Risk Assessment: Breast, Ovarian, and Pancreatic, Version 2.2024. Journal of the National Comprehensive Cancer Network 2023; 21(10):1000–1010. doi: 10.6004/jnccn.2023.0051. [PubMed Abstract]
- Desai NV, Barrows ED, Nielsen SM, et al. Retrospective cohort study on the limitations of direct-to-consumer genetic screening in hereditary breast and ovarian cancer. JCO Precision Oncology 2023; 7:e2200695. [PubMed Abstract]
- Findlay GM, Daza RM, Martin B, et al. Accurate classification of BRCA1 variants with saturation genome editing. Nature 2018; 562(7726):217-222. [PubMed Abstract]
- Garber J, Offit K. Hereditary cancer predisposition syndromes. Journal of Clinical Oncology 2005; 23(2):276–292. [PubMed Abstract]
- Hampel H, Bennett RL, Buchanan A, et al. A practice guideline from the American College of Medical Genetics and Genomics and the National Society of Genetic Counselors: Referral indications for cancer predisposition assessment. Genetics in Medicine 2015; 17(1):70-87. [PubMed Abstract]
- Hassett MJ, Somerfield MR, Baker ER, et al. Management of male breast cancer: ASCO guideline. Journal of Clinical Oncology 2020; 38(16):1849–1863. [PubMed Abstract]
- Horton R, Crawford G, Freeman L, et al. Direct-to-consumer genetic testing. BMJ 2019; 367:l5688. doi: 10.1136/bmj.l5688.
- Kurian AW, Abrahamse P, Furgal A, et al. Germline genetic testing after cancer diagnosis. JAMA 2023; 330(1):43–51. [PubMed Abstract]
- Lindor NM, McMaster ML, Lindor CJ, Greene MH. Concise handbook of familial cancer susceptibility syndromes—second edition. Journal of the National Cancer Institute Monographs 2008; 38:1–93. [PubMed Abstract]
- Lowrance W, Dreicer R, Jarrard DF, et al. Updates to advanced prostate cancer: AUA/SUO guideline (2023). Journal of Urology 2023; 209(6):1082–1090. [PubMed Abstract]
- McGee RB, Nichols KE. Introduction to cancer genetic susceptibility syndromes. Hematology / the Education Program of the American Society of Hematology 2016; 2016(1):293-301. [PubMed Abstract]
- Mersch J, Brown N, Pirzadeh-Miller S, et al. Prevalence of variant reclassification following hereditary cancer genetic testing. JAMA 2018; 320(12):1266-1274. [PubMed Abstract]
- National Comprehensive Cancer Network Genetic/Familial High-Risk Assessment: Colorectal (Version 2.2023). https://www.nccn.org/professionals/physician_gls/pdf/genetics_colon.pdf
- Ramos E, Weissman SM. The dawn of consumer-directed testing. American Journal of Medical Genetics Part C: Seminars in Medical Genetics 2018; 178(1): 89–97. [PubMed Abstract]
- Riley BD, Culver JO, Skrzynia C, et al. Essential elements of genetic cancer risk assessment, counseling, and testing: Updated recommendations of the National Society of Genetic Counselors. Journal of Genetic Counseling 2012; 21(2):151–161. [PubMed Abstract]
- Robson M, Storm C, Weitzel J, et al. American Society of Clinical Oncology Policy Statement update: Genetic and genomic testing for cancer susceptibility. Journal of Clinical Oncology 2010; 28(5):893–901. [PubMed Abstract]
- Sohal DPS, Kennedy EB, Cinar P, et al. Metastatic pancreatic cancer: ASCO guideline update. Journal of Clinical Oncology 2020; 38(27):3217–3230. [PubMed Abstract]
- Spencer DH, Lockwood C, Topol E, et al. Direct-to-consumer genetic testing: Reliable or risky? Clinical Chemistry 2011; 57(12): 1641–1644. doi: 10.1373/clinchem.2011.167197
- Stadler ZK, Schrag D. Genetic testing for cancer susceptibility. JAMA 2023; 330(1):30–32. doi: 10.1001/jama.2023.9474
- Tandy-Connor S, Guiltinan J, Krempely K, et al. False-positive results released by direct-to-consumer genetic tests highlight the importance of clinical confirmation testing for appropriate patient care. Genetics in Medicine 2018; 20(12):1515–1521. [PubMed Abstract]
تهیه و تنظیم: سید طه نوربخش
نظارت و تأیید: فائزه محمدهاشم-متخصص ژنتیک