آنچه در این مطلب خواهید خواند
نکات مهم در رابطه با ژنتیک سرطان کلورکتال
وراثت و خطر
عواملی که نشاندهندهی نقش ژنتیک در سرطان کولورکتال هستند عبارتند از:
(1) سابقهی خانوادگی قوی سرطان کولورکتال و/یا پولیپ؛
(2) سرطانهای اولیهی متعدد در بیمار مبتلا به سرطان کولورکتال؛
(3) وجود سرطانهای دیگر در خانوادهی مرتبط با سندرمهای شناختهشدهای که باعث خطر ارثی سرطان کولورکتال میشوند، مانند سرطان آندومتر؛ و
(4) سن پایین در زمان تشخیص سرطان کولورکتال.
سرطان کولورکتال ارثی معمولاً با الگوی اتوزومال غالب به ارث میرسد، اگرچه دو سندرم با الگوی اتوزومال مغلوب به ارث میرسند (پولیپوز مرتبط با MUTYH و NTHL1). حداقل سه مدل کامپیوتری معتبر برای تخمین احتمال اینکه یک فرد مبتلا به سرطان، حامل یک واریانت بیماریزا در ژن ترمیم عدم تطابق (MMR) مرتبط با سندرم لینچ، شایعترین سندرم ارثی CRC، باشد، در دسترس است. این مدلها شامل مدلهای پیشبینی MMRpro، MMRpredict و PREMM5 (مدل پیشبینی برای جهشهای ژنی) هستند. افرادی که خطر کمی آنها در PREMM5، 2.5٪ یا بیشتر یا در MMRpro و MMRpredict، 5٪ یا بیشتر باشد، برای ارزیابی ژنتیکی و آزمایش توصیه میشوند.
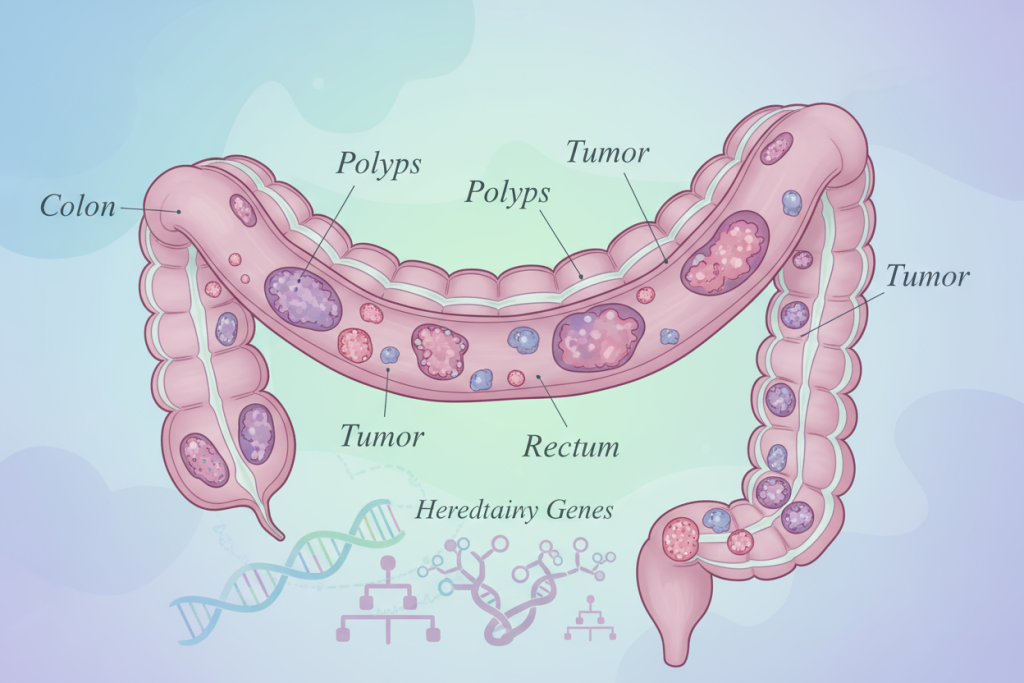
ژنها و سندرمهای مرتبط
سرطان کولورکتال ارثی دو شکل کاملاً شناختهشده دارد:
(1) پولیپوز (شامل پولیپوز آدنوماتوز خانوادگی [FAP] و FAP ضعیفشده [AFAP] که توسط گونههای بیماریزا در ژن APC ایجاد میشوند؛ و پولیپوز مرتبط با MUTYH که توسط گونههای بیماریزا در ژن MUTYH ایجاد میشود)؛ و
(2) سندرم لینچ (که اغلب به عنوان سرطان کولورکتال غیرپولیپی ارثی شناخته میشود) که توسط گونههای بیماریزای رده زایا در ژنهای DNA MMR ( MLH1 ، MSH2 ، MSH6 و PMS2) و EPCAM ایجاد میشود. سایر سندرمهای CRC و ژنهای مرتبط با آنها شامل الیگوپولیپوز (POLE ، POLD1)، NTHL1، سندرم پولیپوز نوجوانان (BMPR1A ،SMAD4)، سندرم کودن (PTEN) و سندرم پوتز-جگرز (STK11) هستند. بسیاری از این سندرمها با سرطانهای خارج روده بزرگ و سایر تظاهرات نیز مرتبط هستند. سندرم پولیپوز دندانهدار، که با ظاهر پولیپهای هیپرپلاستیک مشخص میشود، به نظر میرسد یک جزء خانوادگی داشته باشد، اما اساس ژنتیکی آن ناشناخته است. تاریخچه طبیعی برخی از این سندرمها هنوز در حال توصیف است. بسیاری از خانوادههای دیگر تجمع CRC و/یا آدنومها را نشان میدهند، اما هیچ ارتباط آشکاری با یک سندرم ارثی قابل شناسایی ندارند و در مجموع به عنوان CRC خانوادگی شناخته میشوند. علاوه بر این، اکثر افراد مبتلا به CRC که قبل از 50 سالگی تشخیص داده میشوند و سابقه خانوادگی سرطان ندارند، هیچ گونه بیماریزایی مرتبط با یک سندرم سرطان ارثی ندارند.جستجوهای گسترده در سطح ژنوم، نویدبخش شناسایی آللهای شایع و کمنفوذ حساسیت برای بسیاری از بیماریهای پیچیده، از جمله سرطان کولورکتال (CRCs) هستند، اما کاربرد بالینی این یافتهها همچنان نامشخص است.

مدیریت بالینی
در بسیاری از مراکز، ارزیابی سندرم لینچ برای همه افراد مبتلا به سرطان کولورکتال (CRC) تازه تشخیص داده شده، از طریق آزمایش مولکولی تومور برای ارزیابی کمبود MMR، به استاندارد مراقبت تبدیل شده است. یک رویکرد غربالگری جهانی برای آزمایش تومور پشتیبانی میشود که در آن همه موارد CRC صرف نظر از سن در زمان تشخیص یا برآورده شدن معیارهای بالینی موجود برای سندرم لینچ ارزیابی میشوند. یک رویکرد مقرون به صرفهتر گزارش شده است که در آن همه بیماران 70 سال یا کمتر مبتلا به CRC و بیماران مسنتر که دستورالعملهای اصلاحشده بتسدا را رعایت میکنند، برای سندرم لینچ آزمایش میشوند. ارزیابی تومور اغلب با آزمایش ایمونوهیستوشیمی برای بیان پروتئینهای MMR مرتبط با سندرم لینچ یا آزمایش ناپایداری ریزماهواره (MSI)، آزمایش BRAF و تجزیه و تحلیلهای هیپرمتیلاسیون MLH1 آغاز میشود.کولونوسکوپی برای غربالگری و نظارت بر سرطان کولورکتال (CRC) معمولاً در افراد مبتلا به سندرمهای ارثی سرطان کولورکتال انجام میشود و با بهبود نتایج بقا همراه بوده است. به عنوان مثال، نشان داده شده است که نظارت بر بیماران مبتلا به سندرم لینچ با کولونوسکوپی هر ۱ تا ۲ سال و در یک مطالعه تا ۳ سال، میزان بروز و مرگ و میر سرطان کولورکتال را کاهش میدهد. نظارت خارج رودهای نیز بسته به سایر سرطانهای مرتبط با این سندرم، یک روش اصلی برای برخی از سندرمهای ارثی سرطان کولورکتال است. به عنوان مثال، نشان داده شده است که نظارت منظم آندوسکوپی دوازدهه در بیماران FAP باعث بهبود بقا میشود. همچنین نشان داده شده است که جراحی پیشگیرانه (کولکتومی) باعث بهبود بقا در بیماران مبتلا به FAP میشود. زمان و میزان جراحی کاهشدهنده خطر معمولاً به تعداد پولیپها، اندازه آنها، بافتشناسی و علائم بستگی دارد. برای بیماران مبتلا به سندرم لینچ و تشخیص سرطان کولورکتال (CRC)، برداشتن گسترده با CRC های متاکرونوس کمتر و اقدامات جراحی اضافی برای نئوپلازی کولورکتال نسبت به بیمارانی که تحت برداشتن قطعهای برای CRC قرار میگیرند، همراه است. تصمیم جراحی باید سن بیمار، بیماریهای همراه، مرحله بالینی تومور، عملکرد اسفنکتر و خواستههای بیمار را در نظر بگیرد.عوامل شیمیدرمانی پیشگیرانه نیز در مدیریت FAP و سندرم لینچ مورد مطالعه قرار گرفتهاند. در بیماران FAP، سلکوکسیب و سولینداک با کاهش اندازه و تعداد پولیپ همراه بودهاند. یک کارآزمایی دوسوکور، تصادفی و کنترلشده که اثربخشی سولینداک به همراه یک مهارکننده گیرنده فاکتور رشد اپیدرمی، ارلوتینیب، را در مقایسه با دارونما در بیماران FAP یا AFAP مبتلا به پولیپ اثنیعشر ارزیابی میکند، نشان داد که ارلوتینیب پتانسیل مهار پولیپهای اثنیعشر در بیماران FAP را دارد. یک کارآزمایی در حال انجام مشخص خواهد کرد که آیا دوزهای پایینتر ارلوتینیب به تنهایی به طور قابل توجهی بار پولیپ اثنیعشر را کاهش میدهد یا خیر. در یک کارآزمایی تصادفی بزرگ، نشان داده شد که استفاده از آسپرین (600 میلیگرم در روز) تأثیر پیشگیرانهای بر بروز سرطان در بیماران سندرم لینچ دارد. دوزهای پایینتر در یک مطالعه در حال انجام در حال بررسی هستند.درمانهای جدیدی که سیستم ایمنی را تحریک میکنند، در تومورهای دارای کمبود MMR، از جمله تومورهای مرتبط با سندرم لینچ، ارزیابی شدهاند. نفوذ متراکم ایمنی و محیط غنی از سیتوکین در تومورهای دارای کمبود MMR ممکن است نتایج بالینی را بهبود بخشد. یک مسیر حیاتی که مسئول واسطهگری سرکوب ایمنی ناشی از تومور است، مسیر ایست بازرسی با واسطه مرگ برنامهریزیشده سلولی-1 (PD-1) است. دو مطالعه فاز 2 با استفاده از مهارکنندههای ایست بازرسی ایمنی ضد PD-1 (پمبرولیزوماب و نیوولوماب) نتایج مطلوبی را نشان دادند، از جمله بقای بدون پیشرفت، میزان پاسخ رادیوگرافی و میزان کنترل بیماری در CRC متاستاتیک با کمبود MMR و MSI که در شیمیدرمانی سیتوتوکسیک قبلی پیشرفت کرده بودند. پمبرولیزوماب در سایر سرطانهای غیرکولورکتال با کمبود MMR و MSI نیز فواید مشابهی را نشان داده است، اما در تومورهایی که در ریزماهوارهها پایدار هستند، چنین فایدهای نداشته است.
مسائل روانی-اجتماعی و رفتاری
عوامل روانی-اجتماعی بر تصمیمات مربوط به آزمایش ژنتیک برای خطر سرطان ارثی و استراتژیهای مدیریت ریسک تأثیر میگذارند. میزان استفاده از مشاوره ژنتیک و آزمایش ژنتیک برای سندرم لینچ و FAP در مطالعات مختلف بسیار متفاوت است. عواملی که با مشاوره ژنتیک و انجام آزمایش در خانوادههای مبتلا به سندرم لینچ مرتبط بودهاند عبارتند از: داشتن فرزند، تعداد بستگان مبتلا، خطر درک شده برای ابتلا به سرطان روده بزرگ (CRC) و فراوانی افکار در مورد CRC. مطالعات روانشناسی، سطوح پایینی از پریشانی را، به ویژه در درازمدت، پس از آزمایش ژنتیک برای سندرم لینچ در هر دو گروه حاملان و غیرحاملان نشان دادهاند. با این حال، مطالعات دیگر احتمال افزایش پریشانی پس از آزمایش ژنتیک برای FAP را نشان دادهاند. نشان داده شده است که میزان غربالگری سرطان روده بزرگ و زنان در بین حاملان گونههای بیماریزای MMR در طول سال پس از افشای نتایج افزایش یافته یا حفظ میشود، در حالی که میزان غربالگری در بین غیرحاملان کاهش مییابد. مورد دوم قابل انتظار است زیرا توصیههای غربالگری برای افراد غیرمبتلا همانهایی هستند که برای جمعیت عمومی اعمال میشوند. مطالعاتی که متغیرهای کیفیت زندگی را در بیماران FAP اندازهگیری میکنند، نتایج در محدوده طبیعی را نشان میدهند. با این حال، این مطالعات نشان میدهد که جراحی کاهشدهنده خطر برای FAP ممکن است اثرات منفی بر کیفیت زندگی حداقل برای بخشی از افراد مبتلا داشته باشد. ارتباط بیماران با اعضای خانوادهشان در مورد خطر ارثی سرطان کولورکتال پیچیده است؛ جنسیت، سن و میزان خویشاوندی از جمله عواملی هستند که بر افشای این اطلاعات تأثیر میگذارند. تحقیقات برای درک بهتر و پرداختن به مسائل روانی-اجتماعی و رفتاری در خانوادههای پرخطر در حال انجام است.
تهیه و تنظیم: سیدطه نوربخش
نظارت و تأیید: فائزه محمدهاشم-متخصص ژنتیک